[뉴스인] 마소연 기자 = 부광약품(대표 유희원)은 자회사인 덴마크 CNS(중추신경계) 전문 바이오벤처 '콘테라파마(Contera Pharma)'에서 개발한 레보도파로 유발된 이상운동증(LID) 치료제인 'JM-010'이 최근 식품의약품안전처로부터 개발단계 희귀의약품으로 지정받았다고 6일 밝혔다.
LID는 파킨슨병 환자들에게 치료제인 레보도파를 장기 투여했을 때 60~70%의 환자에서 발생하는 운동장애로, 일상생활에 심각한 장애를 초래하고 환자의 삶의 질을 현저히 저하하지만 아직 치료제가 없는 것으로 알려졌다.
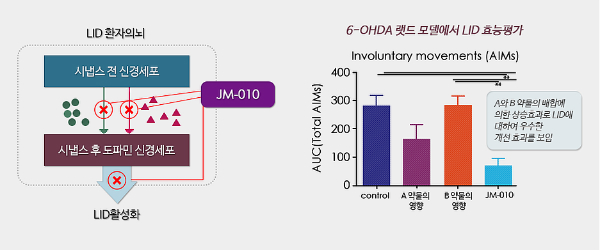
JM-010은 남아프리카공화국에서 수행된 개념증명 임상시험에서 1차 평가변수인 유효성과 안전성 목표를 달성한 것으로 나타났다.
부광약품은 지난해 독일에서 수행된 1상 임상시험이 완료돼 후속 임상시험계획을 진행하고 있으며 올 하반기에 국내 2상 임상시험을 개시하는 것이 목표라고 전했다.
부광약품 관계자는 "JM-010이 개발단계 희귀의약품으로 지정됨에 따라 한국에서의 JM-010 개발에 가속도가 붙을 것으로 전망한다"며 "치료제 보급이 절실한 LID로 고통받는 파킨슨병 환자들에게 희망적인 소식"이라고 말했다.
키워드
#N
마소연 기자
nrubam@newsin.co.kr

